No começo do mês de Setembro de 2025, a Agência Nacional de Vigilância Sanitária (ANVISA) aprovou o registro do Dayvigo® (Lemborexante), medicação com mecanismo de ação específico em vias neuronais para tratamento de insônia, um passo muito importante para um mercado acostumado a tratar essa questão de sono com classe de medicações com níveis de evidência inferiores, ou seja, atualmente o Brasil tem disponível medicações que em guidelines e revisões não alcançam o nível de evidencia 1A para tratamento de insônia, e essa realidade parece ganhar um novo cenário.
A prevalência de insônia na população brasileira é elevada e apresenta variações conforme critérios diagnósticos, faixa etária e metodologia empregada. Estudos nacionais de base populacional indicam que cerca de 35% dos adultos relatam problemas de sono ou sintomas de insônia, com prevalência semelhante quando se utilizam critérios clínicos rigorosos, como queixas frequentes (≥3 vezes por semana) acompanhadas de sofrimento associado.[1-2] Em grandes cidades, como São Paulo, dados longitudinais mostram aumento significativo das queixas de insônia nas últimas décadas: dificuldade para iniciar o sono passou de 13,9% em 1987 para 25% em 2007; dificuldade para manter o sono de 15,8% para 36,5%; e despertar precoce de 10,6% para 26,7%.[3-4] Esses sintomas são mais prevalentes em mulheres e aumentam com a idade. Em relação à incidência, os estudos disponíveis são predominantemente transversais, não permitindo estimativas precisas de novos casos ao longo do tempo. No entanto, a tendência de aumento das queixas de insônia ao longo das últimas décadas sugere crescimento da incidência, especialmente em grandes centros urbanos [4].
Atualmente no Brasil utilizamos medicações antidepressivas com efeitos sedativos, medicações antipsicóticas com efeitos sedativos e hipnóticos, medicações hipnóticas da classe das “drogas Z”, a chegada do Lemborexante, inaugura a disponibilidade de um antagonista duplo dos receptores de orexina (DORA), estes atuam bloqueando de forma competitiva e seletiva os dois subtipos de receptores de orexina, OX1R e OX2R, localizados principalmente no sistema nervoso central.
As orexinas (hipocretinas) são neuropeptídeos produzidos no hipotálamo lateral e exercem papel fundamental na promoção e manutenção do estado de vigília, estimulando múltiplos sistemas neurotransmissores excitatórios, como histamina, noradrenalina, dopamina e serotonina, ao antagonizar simultaneamente OX1R e OX2R (no caso do Lemborexante, OXR2 > OXR1), os DORAs inibem o sinal de excitação promovido pelas orexinas, reduzindo a atividade dos circuitos de vigília e facilitando o início e a manutenção do sono, e não possuem atividade agonista. Esse mecanismo é distinto dos hipnóticos tradicionais, como benzodiazepínicos e Z-drogas, que atuam como moduladores positivos do receptor GABA-A, promovendo sedação por inibição global da atividade neuronal.
As diretrizes norte-americanas mais recentes, como as do Department of Veterans Affairs (2025), reconhecem os DORAs (lemborexante, suvorexante, daridorexante) como opções farmacológicas eficazes para insônia, baseando-se em evidências de múltiplos ensaios clínicos randomizados e meta-análises. O nível de evidência para lemborexante é considerado alto, sustentado por revisões sistemáticas e meta-análises de ensaios clínicos randomizados que demonstram melhora significativa em parâmetros objetivos e subjetivos do sono, como latência para início do sono, eficiência do sono e tempo acordado após início do sono, em comparação ao placebo. Na Europa, lemborexante ainda não está amplamente aprovado ou incorporado nas principais diretrizes clínicas, como as da European Sleep Research Society, no entanto, a evidência científica internacional, incluindo meta-análises e estudos comparativos, posiciona o lemborexante como uma alternativa eficaz e segura, especialmente para pacientes com contraindicação ou intolerância aos tratamentos tradicionais.
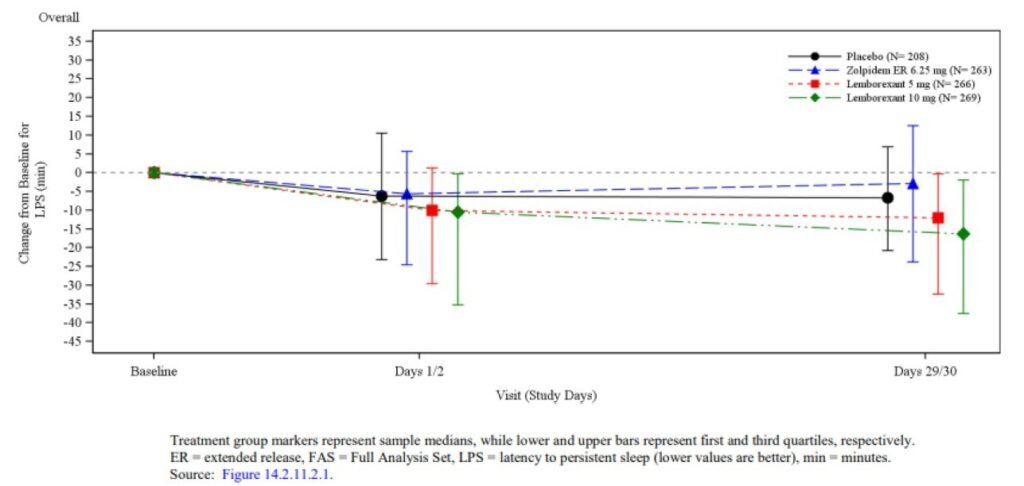
A chegada no mercado brasileiro portanto, permitirá o manejo mais seguro e com maior eficácia inclusive quando comparada a última “menina dos olhos” lançada para sono, o Zolpidem, uma vez que sim, esse fármaco foi comparado ao Zolpidem em termos de eficácia para redução do tempo acordado após o adormecer (WASO), tempo total de sono (TS) e demais parâmetros, demonstrando excelentes resultados.
No Brasil, o Lemborexante estará disponível nas apresentações de 5mg e 10mg, com caixas de 14 e 28 comprimidos, será comercializado como classe de medicação hipnótica/sedativa, portanto, necessitará de Receituário Azul Tipo B, devendo ser utilizado na menor dosagem possível pelo menor tempo possível de tratamento, e nisso, as evidências mostram um tempo de tratamento de seis meses com alvo a ser atingido. Um cuidado importante, o fármaco deve ser tomado já na cama, longe de refeições devido perda eficácia, e o paciente deve ser orientado a ter um tempo total mínimo de cama disponível de sete horas, devido o principal efeito colateral ser sonolência residual e fadiga. O fármaco foi estudo em idades acima de 18 (dezoito) anos e em populações acima de 55 (cinquenta e cinco) anos, tendo sido comprovada sua segurança, não necessitando de ajustes de dose para insuficiência hepática e renal.
Agora nos resta aguardar a data inicial de comercialização, uma vez que falta à indústria responsável pelo Dayvigo ® a determinação do preço máximo ao consumidor e alguns trâmites finais de comercialização, para enfim entendermos como será esse perfil de medicação na nossa população (pouco representada nos estudos internacionais) e principalmente, como será o uso/abuso de tal medicação comparado a sua real eficácia clínica no dia-a-dia, porém, já devemos comemorar que a área do sono está ganhando mais um aliado e está no centro da preocupação das autoridades e indústria farmacêutica. O que o futuro nos reservas com os DORA’s no Brasil ? Já vimos anteriormente que medicações com perfil de ação em sono mexeram com milhões/bilhões de dólares e criaram uma febre de dependência que até hoje estamos lutando contra e o novo cenário parece ser sim mais promissor, mas será que estamos olhando com uma nova lente já contaminada, como foi no passado? A busca incessante por uma pílula que irá resolver os problemas do sono, negligenciando os cuidados com saúde mental, ajustes de rotina e redução de demandas sociais em ciclos ininterruptos de 24hs nunca será uma resposta assertiva, continuaremos com a primeira linha de tratamento sendo a psicoterapia direcionado para o distúrbio do sono, a higiene do sono e o olhar individualizados para os fatores perpetuadores da insônia no indivíduo, uma vez que cuidar do sono é sim olhar para a individualidade, não existe fórmula mágica ou pílula secreta que conseguirá colocar todos para dormir, mas existe sim a possibilidade de aprimorar os cuidados com a saúde do sono.
Por Dr Renan Iegoroff – CRM214250. Pós-Graduado em Neurologia IPEMED/AFYA SP. Medicina do Sono AFIP/SP. Coordenador da Pós-Graduação em Medicina do Sono Inspirali. Membro da AASM, ESRS e da Academia Brasileira do Sono
Referências Bibliográficas:
1.Factors Associated With Sleep Problems and Sleeping Pill Use in Brazilians.Araújo MFS, Souza TA, Medeiros AA, Souza JC, Barbosa IR.Revista De Saude Publica. 2022;56:68. doi:10.11606/s1518-8787.2022056004088.
2.Prevalence of Insomnia and Associated Socio-Demographic Factors in a Brazilian Community: The Bambuí Study.Rocha FL, Guerra HL, Lima-Costa MF.Sleep Medicine. 2002;3(2):121-6. doi:10.1016/s1389-9457(01)00119-8
3.Sleep Habits and Complaints of Adults in the City of São Paulo, Brazil, in 1987 and 1995.Pires ML, Benedito-Silva AA, Mello MT, Pompeia Sdel G, Tufik S.Brazilian Journal of Medical and Biological Research = Revista Brasileira De Pesquisas Medicas E Biologicas. 2007;40(11):1505-15.
4.Increasing Trends of Sleep Complaints in the City of Sao Paulo, Brazil.Santos-Silva R, Bittencourt LR, Pires ML, et al.Sleep Medicine. 2010;11(6):520-4. doi:10.1016/j.sleep.2009.12.011.
Rosenberg R, Murphy P, Zammit G, Mayleben D, Kumar D, Dhadda S, Filippov G, LoPresti A, Moline M. Comparison of Lemborexant With Placebo and Zolpidem Tartrate Extended Release for the Treatment of Older Adults With Insomnia Disorder: A Phase 3 Randomized Clinical Trial. JAMA Netw Open. 2019 Dec 2;2(12):e1918254. doi: 10.1001/jamanetworkopen.2019.18254. Erratum in: JAMA Netw Open. 2020 Apr 1;3(4):e206497. doi: 10.1001/jamanetworkopen.2020.6497. Erratum in: JAMA Netw Open. 2021 Aug 2;4(8):e2127643. doi: 10.1001/jamanetworkopen.2021.27643. PMID: 31880796; PMCID: PMC6991236.
